लेखक:
Louise Ward
निर्माण की तारीख:
11 फ़रवरी 2021
डेट अपडेट करें:
1 जुलाई 2024

विषय
एक परमाणु का आकार इतना छोटा होता है कि किसी रासायनिक यौगिक की परमाणु संख्या को सटीक रूप से मापना मुश्किल होता है। पदार्थों की मात्रा को सटीक रूप से मापने में सक्षम होने के लिए, वैज्ञानिक एक निर्दिष्ट संख्या में परमाणुओं का प्रतिनिधित्व करने के लिए तिल की एक इकाई का उपयोग करते हैं। 12 कार्बन समस्थानिक के 12 ग्राम में निहित कार्बन परमाणुओं की संख्या के बराबर पदार्थ के एक तिल को परिभाषित किया गया है, जो लगभग 6,022 x 10 परमाणु है। इस मान को एवोगैड्रो संख्या या एवोगैड्रो स्थिरांक कहा जाता है। इसे किसी भी तत्व के 1 मोल में परमाणुओं की संख्या के रूप में भी जाना जाता है, और किसी पदार्थ के द्रव्यमान के 1 मोल को उस पदार्थ का दाढ़ द्रव्यमान कहा जाता है।
कदम
विधि 1 की 2: एक तत्व के दाढ़ द्रव्यमान की गणना करें
दाढ़ द्रव्यमान की परिभाषा। किसी पदार्थ का मोलर द्रव्यमान उस पदार्थ के एक मोल का द्रव्यमान (ग्राम में) होता है। एक तत्व के दाढ़ द्रव्यमान की गणना करने के लिए, रूपांतरण कारक ग्राम प्रति मोल (जी / मोल) द्वारा अपने परमाणु द्रव्यमान को गुणा करें।
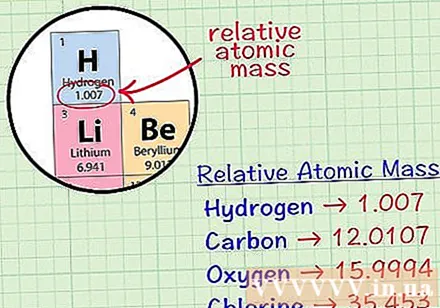
किसी तत्व का औसत घन परमाणु ज्ञात कीजिए। एक तत्व का औसत द्रव्यमान परमाणु, परमाणु इकाइयों में एक नमूना में औसत द्रव्यमान होता है, जिसमें उस तत्व के सभी समस्थानिक शामिल होते हैं। यह जानकारी अक्सर तत्वों की आवर्त सारणी पर दी जाती है। एक तत्व का पता लगाने से, आप तत्व के रासायनिक प्रतीक के ठीक नीचे लिखा एक औसत घन परमाणु पा सकते हैं। यह मान पूर्णांक नहीं है, लेकिन दशमलव के साथ एक संख्या है।- उदाहरण के लिए, हाइड्रोजन के साथ, औसत द्रव्यमान परमाणु 1.007 है; कार्बन का औसत घन परमाणु 12,0107 है; ऑक्सीजन का औसत द्रव्यमान परमाणु 15,9994 है; क्लोरीन का औसत परमाणु द्रव्यमान 35,453 है।

दाढ़ द्रव्यमान स्थिरांक द्वारा औसत द्रव्यमान परमाणु को गुणा करें। मोलर ग्लाइड की इकाई को 0.001 किलोग्राम प्रति मोल या 1 ग्राम प्रति मोल के रूप में परिभाषित किया गया है। माध्य द्रव्यमान परमाणु और दाढ़ द्रव्यमान का गुणनफल परमाणु द्रव्यमान की इकाई को प्रति ग्राम ग्राम में परिवर्तित करता है, इसलिए हाइड्रोजन का दाढ़ द्रव्यमान 1.007 ग्राम प्रति मोल होगा, कार्बन का 12। , 0107 ग्राम प्रति मोल, ऑक्सीजन की मात्रा 15,9995 ग्राम प्रति मोल है और क्लोरीन 35,453 ग्राम प्रति मोल है।- कुछ तत्व प्रकृति में मौजूद होते हैं, अणु समान परमाणुओं के दो या अधिक होते हैं। यही है, यदि आप एक से अधिक परमाणु से बने यौगिकों के दाढ़ द्रव्यमान की गणना करना चाहते हैं, जैसे हाइड्रोजन गैस, ऑक्सीजन गैस या क्लोरीन गैस, तो आपको यौगिक के औसत परमाणु द्रव्यमान को निर्धारित करने और इस मूल्य को गुणा करने की आवश्यकता है। दाढ़ द्रव्यमान स्थिरांक के साथ, '' तब '' उत्पाद को आप केवल 2 से मिलाते हैं।
- एच के साथ2: 1,007 x 2 = 2,014 ग्राम प्रति मोल; ओ के लिए2: 15,9994 x 2 = 31,9988 ग्राम प्रति मोल; और सीएल2: 35,453 x 2 = 70,096 ग्राम प्रति मोल।
विधि 2 की 2: यौगिक के दाढ़ द्रव्यमान की गणना करें

यौगिक के संरचनात्मक सूत्र का निर्धारण करें। किसी पदार्थ का संरचनात्मक सूत्र उस यौगिक को बनाने वाले प्रत्येक तत्व की परमाणु संख्या देता है। (यह जानकारी सभी संदर्भ पुस्तकों में उपलब्ध है)। उदाहरण के लिए, हाइड्रोक्लोरिक एसिड का रासायनिक सूत्र एचसीएल है; ग्लूकोज की C है6एच12हे6। इस संरचनात्मक सूत्र के साथ, हम प्रत्येक प्रकार के परमाणु की संख्या निर्धारित कर सकते हैं जो विचार के तहत यौगिक का निर्माण करते हैं।- जहां एचसीएल में एक हाइड्रोजन परमाणु और एक क्लोरीन परमाणु होता है।
- ग्लूकोज चीनी अणु सी6एच12हे6 6 कार्बन परमाणु, 12 हाइड्रोजन परमाणु और 6 ऑक्सीजन परमाणु हैं।
प्रत्येक घटक तत्व का औसत द्रव्यमान परमाणु निर्धारित करें। यौगिक में मौजूद प्रत्येक तत्व का औसत द्रव्यमान परमाणु ज्ञात करने के लिए आवर्त सारणी का उपयोग करें। औसत द्रव्यमान परमाणु आमतौर पर आवर्त सारणी पर तत्व के रासायनिक प्रतीक के तहत लिखा जाता है। एक तत्व के दाढ़ द्रव्यमान की गणना के समान, 1 ग्राम / मोल द्वारा औसत द्रव्यमान परमाणु को गुणा करें।
- हाइड्रोक्लोरिक एसिड बनाने वाले तत्वों का औसत द्रव्यमान परमाणु इस प्रकार है: हाइड्रोजन 1,007 g / mol और क्लोरीन 35,453 g / mol।
- ग्लूकोज अणु बनाने वाले तत्वों का औसत द्रव्यमान परमाणु है: कार्बन, 12,017 ग्राम / मोल; हाइड्रोजन, 1,007 ग्राम / मोल; और ऑक्सीजन, 15.9995 ग्राम / मोल।
प्रत्येक घटक तत्व के दाढ़ द्रव्यमान की गणना करें। किसी यौगिक में किसी तत्व के द्रव्यमान परमाणु को गुणा करने से उस यौगिक में योगदान होता है जो यौगिक में तत्व का औसत द्रव्यमान देता है।
- हाइड्रोक्लोरिक एसिड, HCl के मामले में, तत्व हाइड्रोजन का दाढ़ द्रव्यमान 1,007 g / mol है, और क्लोरीन का 35,453 g / mol है।
- ग्लूकोज के मामले में, सी6एच12हे6, प्रत्येक तत्व का दाढ़ द्रव्यमान निम्नानुसार है: कार्बन, 12,0107 x 6 = 72,0642 ग्राम / मोल; हाइड्रोजन, 1,007 x 12 = 12,084 ग्राम / मोल; ऑक्सीजन, 15,9995 x 6 = 95,9964 ग्राम / मोल।
घटक तत्वों का कुल दाढ़ द्रव्यमान। कंपोस्टिंग तत्वों का कुल दाढ़ द्रव्यमान यौगिक का दाढ़ द्रव्यमान है।पिछले चरण में हमने यौगिक में मौजूद प्रत्येक तत्व के दाढ़ द्रव्यमान की गणना की, इस चरण में हमें बस इन सभी मूल्यों को एक साथ जोड़ने की आवश्यकता है।
- हाइड्रोक्लोरिक एसिड का मोलर द्रव्यमान 1,007 + 35,453 = 36,460 ग्राम / मोल है। 36.46 ग्राम हाइड्रोक्लोरिक एसिड के 1 मोल का द्रव्यमान है।
- ग्लूकोज का मोलर द्रव्यमान 72,0642 + 12,084 + 95,9964 = 180,1446 ग्राम / मोल है। तो ग्लूकोज के प्रत्येक मोल का द्रव्यमान 180.14 ग्राम होता है।
सलाह
- हालांकि ज्यादातर मामलों में औसत द्रव्यमान परमाणु 1 भाग 1000 (4 दशमलव स्थानों) में दर्ज किया जाता है, प्रयोगशालाओं में, दाढ़ द्रव्यमान अक्सर 2 दशमलव स्थानों तक कम हो जाता है, बड़े अणुओं के लिए भी कभी-कभी कम। इसलिए, प्रयोगशाला मामले में, हाइड्रोक्लोरिक एसिड के मोलर द्रव्यमान को 36.46 ग्राम प्रति मोल, ग्लूकोज 180.14 ग्राम प्रति मोल के रूप में लिखा जा सकता है।
जिसकी आपको जरूरत है
- रासायनिक संदर्भ पुस्तक या तत्वों की आवर्त सारणी
- संगणक