लेखक:
Eric Farmer
निर्माण की तारीख:
10 जुलूस 2021
डेट अपडेट करें:
1 जुलाई 2024

विषय
- कदम
- विधि 1 में से 2: परमाणुओं में न्यूट्रॉन की संख्या निर्धारित करना (आइसोटोप नहीं)
- विधि २ का २: आइसोटोप में न्यूट्रॉन की संख्या का निर्धारण
- टिप्स
एक ही तत्व के परमाणुओं में, प्रोटॉन की संख्या स्थिर होती है, जबकि न्यूट्रॉन की संख्या भिन्न हो सकती है।किसी विशेष परमाणु में कितने न्यूट्रॉन होते हैं, यह जानकर आप यह निर्धारित कर सकते हैं कि यह एक नियमित परमाणु है या एक समस्थानिक जिसमें कम या अधिक न्यूट्रॉन होंगे। एक परमाणु में न्यूट्रॉन की संख्या निर्धारित करना काफी सरल है। परमाणु या समस्थानिक में न्यूट्रॉन की संख्या की गणना करने के लिए आपको केवल हमारे निर्देशों का पालन करना है और आवर्त सारणी को संभाल कर रखना है।
कदम
विधि 1 में से 2: परमाणुओं में न्यूट्रॉन की संख्या निर्धारित करना (आइसोटोप नहीं)
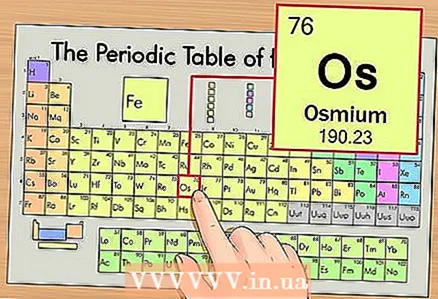 1 आवर्त सारणी पर तत्व का पता लगाएं। एक उदाहरण के रूप में, हम ऑस्मियम (Os) पर विचार करेंगे, जो छठे आवर्त (ऊपर से छठी पंक्ति) में है।
1 आवर्त सारणी पर तत्व का पता लगाएं। एक उदाहरण के रूप में, हम ऑस्मियम (Os) पर विचार करेंगे, जो छठे आवर्त (ऊपर से छठी पंक्ति) में है।  2 तत्व का परमाणु क्रमांक ज्ञात कीजिए। यह, एक नियम के रूप में, किसी तत्व के सेल में सबसे अधिक ध्यान देने योग्य संख्या है और आमतौर पर इसके प्रतीक के ऊपर स्थित होता है (आवर्त सारणी के संस्करण में जिसे हम अपने उदाहरण में उपयोग करते हैं, कोई अन्य संख्या नहीं है)। परमाणु क्रमांक उस तत्व के एक परमाणु में प्रोटॉनों की संख्या है। ऑस्मियम के लिए यह संख्या 76 होती है, यानी एक ऑस्मियम परमाणु में 76 प्रोटॉन होते हैं।
2 तत्व का परमाणु क्रमांक ज्ञात कीजिए। यह, एक नियम के रूप में, किसी तत्व के सेल में सबसे अधिक ध्यान देने योग्य संख्या है और आमतौर पर इसके प्रतीक के ऊपर स्थित होता है (आवर्त सारणी के संस्करण में जिसे हम अपने उदाहरण में उपयोग करते हैं, कोई अन्य संख्या नहीं है)। परमाणु क्रमांक उस तत्व के एक परमाणु में प्रोटॉनों की संख्या है। ऑस्मियम के लिए यह संख्या 76 होती है, यानी एक ऑस्मियम परमाणु में 76 प्रोटॉन होते हैं। - प्रोटॉन की संख्या अपरिवर्तित रहती है, और यही तत्व को एक तत्व बनाता है।
 3 किसी तत्व का परमाणु द्रव्यमान ज्ञात कीजिए। यह संख्या आमतौर पर तत्व प्रतीक के नीचे पाई जाती है। कृपया ध्यान दें कि हमारे उदाहरण में आवर्त सारणी के संस्करण में, परमाणु द्रव्यमान नहीं दिया गया है (यह हमेशा ऐसा नहीं होता है, आवर्त सारणी के कई संस्करणों में, परमाणु द्रव्यमान का संकेत दिया जाता है)। ऑस्मियम का परमाणु द्रव्यमान 190.23 है।
3 किसी तत्व का परमाणु द्रव्यमान ज्ञात कीजिए। यह संख्या आमतौर पर तत्व प्रतीक के नीचे पाई जाती है। कृपया ध्यान दें कि हमारे उदाहरण में आवर्त सारणी के संस्करण में, परमाणु द्रव्यमान नहीं दिया गया है (यह हमेशा ऐसा नहीं होता है, आवर्त सारणी के कई संस्करणों में, परमाणु द्रव्यमान का संकेत दिया जाता है)। ऑस्मियम का परमाणु द्रव्यमान 190.23 है।  4 परमाणु द्रव्यमान को निकटतम पूर्ण संख्या में गोल करें। हमारे उदाहरण में, 190.23 को 190 तक पूर्णांकित किया गया है।
4 परमाणु द्रव्यमान को निकटतम पूर्ण संख्या में गोल करें। हमारे उदाहरण में, 190.23 को 190 तक पूर्णांकित किया गया है। - परमाणु द्रव्यमान किसी विशेष तत्व के समस्थानिकों की औसत संख्या है, आमतौर पर इसे पूर्णांक के रूप में व्यक्त नहीं किया जाता है।
 5 परमाणु द्रव्यमान से परमाणु संख्या घटाएं। चूंकि प्रोटॉन और न्यूट्रॉन परमाणु द्रव्यमान के पूर्ण भाग के लिए खाते हैं, परमाणु द्रव्यमान से प्रोटॉन की संख्या (यानी, परमाणु संख्या, जो प्रोटॉन की संख्या के बराबर है) को घटाकर परमाणु में न्यूट्रॉन की संख्या देता है। दशमलव बिंदु के बाद की संख्या एक परमाणु में इलेक्ट्रॉनों के बहुत छोटे द्रव्यमान को दर्शाती है। हमारे उदाहरण में: 190 (परमाणु भार) - 76 (प्रोटॉन की संख्या) = 114 (न्यूट्रॉन की संख्या)।
5 परमाणु द्रव्यमान से परमाणु संख्या घटाएं। चूंकि प्रोटॉन और न्यूट्रॉन परमाणु द्रव्यमान के पूर्ण भाग के लिए खाते हैं, परमाणु द्रव्यमान से प्रोटॉन की संख्या (यानी, परमाणु संख्या, जो प्रोटॉन की संख्या के बराबर है) को घटाकर परमाणु में न्यूट्रॉन की संख्या देता है। दशमलव बिंदु के बाद की संख्या एक परमाणु में इलेक्ट्रॉनों के बहुत छोटे द्रव्यमान को दर्शाती है। हमारे उदाहरण में: 190 (परमाणु भार) - 76 (प्रोटॉन की संख्या) = 114 (न्यूट्रॉन की संख्या)। 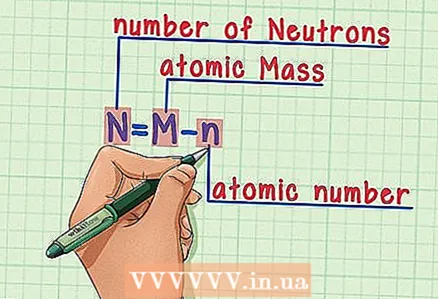 6 सूत्र याद रखें। भविष्य में न्यूट्रॉन की संख्या ज्ञात करने के लिए, बस इस सूत्र का उपयोग करें:
6 सूत्र याद रखें। भविष्य में न्यूट्रॉन की संख्या ज्ञात करने के लिए, बस इस सूत्र का उपयोग करें: - एन = एम - एन
- एन = न्यूट्रॉन की संख्या
- एम = परमाणु द्रव्यमान
- एन = परमाणु संख्या
- एन = एम - एन
विधि २ का २: आइसोटोप में न्यूट्रॉन की संख्या का निर्धारण
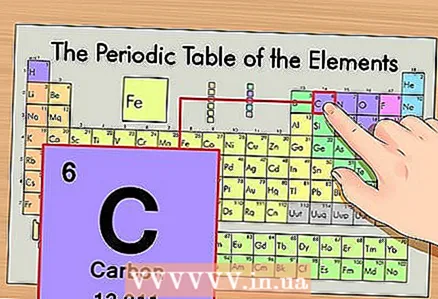 1 आवर्त सारणी पर तत्व का पता लगाएं। एक उदाहरण के रूप में, हम कार्बन 14C के समस्थानिक पर विचार करेंगे। चूँकि गैर-समस्थानिक कार्बन 14C सिर्फ कार्बन C है, आवर्त सारणी (ऊपर से दूसरी अवधि या दूसरी पंक्ति) पर कार्बन खोजें।
1 आवर्त सारणी पर तत्व का पता लगाएं। एक उदाहरण के रूप में, हम कार्बन 14C के समस्थानिक पर विचार करेंगे। चूँकि गैर-समस्थानिक कार्बन 14C सिर्फ कार्बन C है, आवर्त सारणी (ऊपर से दूसरी अवधि या दूसरी पंक्ति) पर कार्बन खोजें। 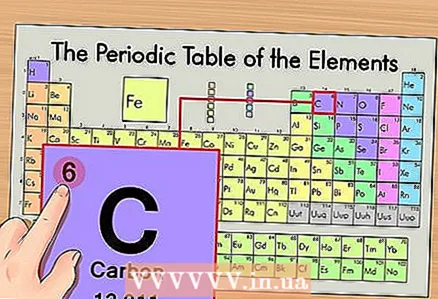 2 तत्व का परमाणु क्रमांक ज्ञात कीजिए। यह, एक नियम के रूप में, किसी तत्व के सेल में सबसे अधिक ध्यान देने योग्य संख्या है और आमतौर पर इसके प्रतीक के ऊपर स्थित होता है (आवर्त सारणी के संस्करण में जिसे हम अपने उदाहरण में उपयोग करते हैं, कोई अन्य संख्या नहीं है)। परमाणु क्रमांक उस तत्व के एक परमाणु में प्रोटॉनों की संख्या है। कार्बन संख्या 6 है, जिसका अर्थ है कि एक कार्बन में छह प्रोटॉन होते हैं।
2 तत्व का परमाणु क्रमांक ज्ञात कीजिए। यह, एक नियम के रूप में, किसी तत्व के सेल में सबसे अधिक ध्यान देने योग्य संख्या है और आमतौर पर इसके प्रतीक के ऊपर स्थित होता है (आवर्त सारणी के संस्करण में जिसे हम अपने उदाहरण में उपयोग करते हैं, कोई अन्य संख्या नहीं है)। परमाणु क्रमांक उस तत्व के एक परमाणु में प्रोटॉनों की संख्या है। कार्बन संख्या 6 है, जिसका अर्थ है कि एक कार्बन में छह प्रोटॉन होते हैं। 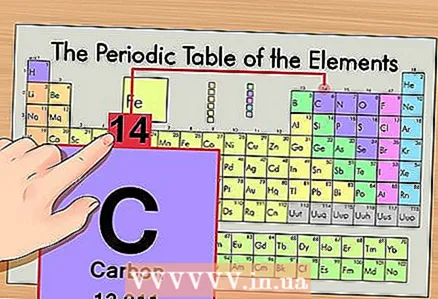 3 परमाणु द्रव्यमान ज्ञात कीजिए। समस्थानिकों के मामले में, यह करना बहुत आसान है, क्योंकि उनका नाम उनके परमाणु द्रव्यमान के अनुसार रखा गया है। हमारे मामले में, कार्बन 14C का परमाणु द्रव्यमान 14 है। अब हम समस्थानिक के परमाणु द्रव्यमान को जानते हैं; बाद की गणना प्रक्रिया परमाणुओं (आइसोटोप नहीं) में न्यूट्रॉन की संख्या निर्धारित करने के समान है।
3 परमाणु द्रव्यमान ज्ञात कीजिए। समस्थानिकों के मामले में, यह करना बहुत आसान है, क्योंकि उनका नाम उनके परमाणु द्रव्यमान के अनुसार रखा गया है। हमारे मामले में, कार्बन 14C का परमाणु द्रव्यमान 14 है। अब हम समस्थानिक के परमाणु द्रव्यमान को जानते हैं; बाद की गणना प्रक्रिया परमाणुओं (आइसोटोप नहीं) में न्यूट्रॉन की संख्या निर्धारित करने के समान है।  4 परमाणु द्रव्यमान से परमाणु संख्या घटाएं। चूंकि प्रोटॉन और न्यूट्रॉन परमाणु द्रव्यमान के पूर्ण भाग के लिए खाते हैं, परमाणु द्रव्यमान से प्रोटॉन की संख्या (यानी, परमाणु संख्या, जो प्रोटॉन की संख्या के बराबर है) को घटाकर परमाणु में न्यूट्रॉन की संख्या देता है। हमारे उदाहरण में: 14 (परमाणु द्रव्यमान) - 6 (प्रोटॉन की संख्या) = 8 (न्यूट्रॉन की संख्या)।
4 परमाणु द्रव्यमान से परमाणु संख्या घटाएं। चूंकि प्रोटॉन और न्यूट्रॉन परमाणु द्रव्यमान के पूर्ण भाग के लिए खाते हैं, परमाणु द्रव्यमान से प्रोटॉन की संख्या (यानी, परमाणु संख्या, जो प्रोटॉन की संख्या के बराबर है) को घटाकर परमाणु में न्यूट्रॉन की संख्या देता है। हमारे उदाहरण में: 14 (परमाणु द्रव्यमान) - 6 (प्रोटॉन की संख्या) = 8 (न्यूट्रॉन की संख्या)। 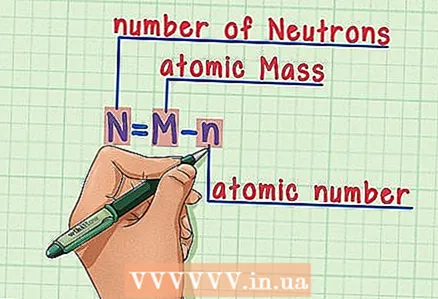 5 सूत्र याद रखें। भविष्य में न्यूट्रॉन की संख्या ज्ञात करने के लिए, बस इस सूत्र का उपयोग करें:
5 सूत्र याद रखें। भविष्य में न्यूट्रॉन की संख्या ज्ञात करने के लिए, बस इस सूत्र का उपयोग करें: - एन = एम - एन
- एन = न्यूट्रॉन की संख्या
- एम = परमाणु द्रव्यमान
- n = परमाणु क्रमांक
- एन = एम - एन
टिप्स
- प्रोटॉन और न्यूट्रॉन तत्वों का लगभग पूर्ण द्रव्यमान बनाते हैं, जबकि इलेक्ट्रॉन और अन्य कण अत्यंत महत्वहीन द्रव्यमान बनाते हैं (यह द्रव्यमान शून्य हो जाता है)।चूँकि एक प्रोटॉन का द्रव्यमान लगभग एक न्यूट्रॉन के बराबर होता है, और परमाणु क्रमांक प्रोटॉनों की संख्या है, इसलिए आप केवल कुल द्रव्यमान से प्रोटॉन की संख्या घटा सकते हैं।
- ऑस्मियम - कमरे के तापमान पर एक ठोस अवस्था में एक धातु, इसका नाम ग्रीक शब्द "ओस्मे" - गंध से मिला है।
- यदि आप सुनिश्चित नहीं हैं कि आवर्त सारणी में किसी संख्या का क्या अर्थ है, तो याद रखें: तालिका आमतौर पर एक परमाणु संख्या (यानी, प्रोटॉन की संख्या) के आसपास बनाई जाती है, जो 1 (हाइड्रोजन) से शुरू होती है और बाएं से दाएं एक इकाई बढ़ती है , 118 (ओगेनेसन) के साथ समाप्त। ऐसा इसलिए है क्योंकि एक परमाणु में प्रोटॉन की संख्या ही तत्व को निर्धारित करती है, और ऐसी संख्या तत्वों को व्यवस्थित करने का सबसे आसान तरीका है (उदाहरण के लिए, 2 प्रोटॉन वाला परमाणु हमेशा हीलियम होता है, जैसे 79 प्रोटॉन वाला परमाणु हमेशा सोना होता है) )



