लेखक:
Marcus Baldwin
निर्माण की तारीख:
20 जून 2021
डेट अपडेट करें:
1 जुलाई 2024

विषय
- कदम
- 5 में से विधि 1 : अध्ययन की अच्छी आदतें
- 5 की विधि 2 : परमाणु संरचना को समझना
- विधि 3 की 5: रासायनिक प्रतिक्रियाओं की गणना
- 5 की विधि 4 : कैलकुलेशन
- विधि 5 की 5: रसायन विज्ञान की भाषा
- टिप्स
सामान्य रसायन विज्ञान परीक्षा पास करने के लिए, विषय की मूल बातें जानना, गिनने में सक्षम होना, अधिक जटिल समस्याओं के लिए कैलकुलेटर का उपयोग करना और कुछ नया सीखने के लिए तैयार रहना महत्वपूर्ण है। रसायन विज्ञान पदार्थों और उनके गुणों का अध्ययन करता है। हमारे चारों ओर सब कुछ रसायन विज्ञान के बारे में है, यहां तक कि सबसे सरल चीजें जिन्हें हम हल्के में लेते हैं, जैसे कि हम जो पानी पीते हैं और जिस हवा में हम सांस लेते हैं। अपने आस-पास की हर चीज़ की खोज के लिए तैयार हो जाइए। केमिस्ट्री को जानना मजेदार होगा।
कदम
5 में से विधि 1 : अध्ययन की अच्छी आदतें
 1 अपने शिक्षक या शिक्षक से मिलें। परीक्षा को सफलतापूर्वक पास करने के लिए, आपको अपने प्रशिक्षक को जानना चाहिए और उसे बताना चाहिए कि आपके लिए क्या कठिन है।
1 अपने शिक्षक या शिक्षक से मिलें। परीक्षा को सफलतापूर्वक पास करने के लिए, आपको अपने प्रशिक्षक को जानना चाहिए और उसे बताना चाहिए कि आपके लिए क्या कठिन है। - यदि छात्रों को सहायता की आवश्यकता हो तो कई शिक्षकों से कक्षा के बाहर संपर्क किया जा सकता है। इसके अलावा, उनके पास आमतौर पर व्यवस्थित प्रकाशन होते हैं।
 2 अभ्यास करने के लिए एक समूह प्राप्त करें। शर्मिंदा न हों कि रसायन शास्त्र आपके लिए कठिन है। यह विषय लगभग सभी के लिए कठिन है।
2 अभ्यास करने के लिए एक समूह प्राप्त करें। शर्मिंदा न हों कि रसायन शास्त्र आपके लिए कठिन है। यह विषय लगभग सभी के लिए कठिन है। - एक समूह में काम करते हुए, जो लोग किसी विषय को जल्दी से समझ सकते हैं, वे उसे दूसरों को समझाएंगे। विभाजन और जीत।
 3 ट्यूटोरियल में प्रासंगिक पैराग्राफ पढ़ें। रसायन विज्ञान की पाठ्यपुस्तकें सबसे रोमांचक पठन नहीं हैं, लेकिन आपको सामग्री को ध्यान से पढ़ना चाहिए और उस पाठ को हाइलाइट करना चाहिए जिसे आप नहीं समझते हैं। उन प्रश्नों और अवधारणाओं की एक सूची बनाएं जिन्हें समझना आपके लिए कठिन हो।
3 ट्यूटोरियल में प्रासंगिक पैराग्राफ पढ़ें। रसायन विज्ञान की पाठ्यपुस्तकें सबसे रोमांचक पठन नहीं हैं, लेकिन आपको सामग्री को ध्यान से पढ़ना चाहिए और उस पाठ को हाइलाइट करना चाहिए जिसे आप नहीं समझते हैं। उन प्रश्नों और अवधारणाओं की एक सूची बनाएं जिन्हें समझना आपके लिए कठिन हो। - बाद में नए सिरे से इन हिस्सों में वापस आएं। यदि आपको अभी भी यह मुश्किल लगता है, तो समूह में विषय पर चर्चा करें या अपने शिक्षक से मदद मांगें।
 4 पैराग्राफ के बाद प्रश्नों के उत्तर दें। यहां तक कि अगर बहुत सारी सामग्री है, तो भी आप जितना सोचते हैं उससे ज्यादा याद कर सकते हैं। अध्याय के अंत में प्रश्नों के उत्तर देने का प्रयास करें।
4 पैराग्राफ के बाद प्रश्नों के उत्तर दें। यहां तक कि अगर बहुत सारी सामग्री है, तो भी आप जितना सोचते हैं उससे ज्यादा याद कर सकते हैं। अध्याय के अंत में प्रश्नों के उत्तर देने का प्रयास करें। - कभी-कभी पाठ्यपुस्तकों के अंत में व्याख्यात्मक सामग्री होती है जो सही समाधान का वर्णन करती है। इससे आपको यह समझने में मदद मिलेगी कि आप तर्क करने में कहां चूक गए।
 5 चार्ट, छवियों और तालिकाओं की जांच करें। पाठ्यपुस्तकें सूचना देने के दृश्य साधनों का उपयोग करती हैं।
5 चार्ट, छवियों और तालिकाओं की जांच करें। पाठ्यपुस्तकें सूचना देने के दृश्य साधनों का उपयोग करती हैं। - चित्रों और आरेखों को देखें। यह आपको कुछ अवधारणाओं को बेहतर ढंग से समझने की अनुमति देगा।
 6 एक टेप रिकॉर्डर पर व्याख्यान रिकॉर्ड करने की अनुमति के लिए अपने प्रशिक्षक से पूछें। जानकारी लिखना और फिर भी ब्लैकबोर्ड को देखना मुश्किल है, खासकर जब रसायन विज्ञान जैसे जटिल विषय की बात आती है।
6 एक टेप रिकॉर्डर पर व्याख्यान रिकॉर्ड करने की अनुमति के लिए अपने प्रशिक्षक से पूछें। जानकारी लिखना और फिर भी ब्लैकबोर्ड को देखना मुश्किल है, खासकर जब रसायन विज्ञान जैसे जटिल विषय की बात आती है।  7 पिछले परीक्षा के प्रश्न देखें। कभी-कभी छात्रों को ऐसे प्रश्न दिए जाते हैं जो पिछले वर्षों में परीक्षाओं में आए थे ताकि वे बेहतर तैयारी कर सकें।
7 पिछले परीक्षा के प्रश्न देखें। कभी-कभी छात्रों को ऐसे प्रश्न दिए जाते हैं जो पिछले वर्षों में परीक्षाओं में आए थे ताकि वे बेहतर तैयारी कर सकें। - उत्तर याद न रखें। रसायन विज्ञान एक ऐसा विषय है, जहां किसी प्रश्न का उत्तर देने के लिए, यह समझना महत्वपूर्ण है कि यह किस बारे में है, न कि केवल याद किए गए पाठ को दोहराएं।
 8 ऑनलाइन शिक्षण संसाधनों का लाभ उठाएं। उन सभी साइटों पर जाएँ जिनकी आपके प्रशिक्षक ने सिफारिश की है।
8 ऑनलाइन शिक्षण संसाधनों का लाभ उठाएं। उन सभी साइटों पर जाएँ जिनकी आपके प्रशिक्षक ने सिफारिश की है।
5 की विधि 2 : परमाणु संरचना को समझना
 1 सबसे सरल इमारत से शुरू करें। एक परीक्षा बनने के लिए, आपको यह जानना होगा कि सब कुछ किस चीज से बना है, जो पदार्थ है और जिसका द्रव्यमान है।
1 सबसे सरल इमारत से शुरू करें। एक परीक्षा बनने के लिए, आपको यह जानना होगा कि सब कुछ किस चीज से बना है, जो पदार्थ है और जिसका द्रव्यमान है। - यह सब परमाणु की संरचना को समझने से शुरू होता है। बाकी सब ऊपर से जोड़ा जाएगा। परमाणु के बारे में सभी जानकारी का बहुत ध्यान से अध्ययन करना महत्वपूर्ण है।
 2 परमाणु की अवधारणा की जाँच करें। एक परमाणु हर चीज का सबसे छोटा "ईंट" होता है जिसमें द्रव्यमान होता है, जिसमें ऐसे पदार्थ भी शामिल होते हैं जिन्हें हम हमेशा नहीं देख सकते हैं (उदाहरण के लिए, गैसें)। लेकिन एक परमाणु में भी छोटे-छोटे कण होते हैं जो इसकी संरचना बनाते हैं..
2 परमाणु की अवधारणा की जाँच करें। एक परमाणु हर चीज का सबसे छोटा "ईंट" होता है जिसमें द्रव्यमान होता है, जिसमें ऐसे पदार्थ भी शामिल होते हैं जिन्हें हम हमेशा नहीं देख सकते हैं (उदाहरण के लिए, गैसें)। लेकिन एक परमाणु में भी छोटे-छोटे कण होते हैं जो इसकी संरचना बनाते हैं.. - एक परमाणु में तीन भाग होते हैं - न्यूट्रॉन, प्रोटॉन और इलेक्ट्रॉन। परमाणु के केंद्र को नाभिक कहते हैं। नाभिक न्यूट्रॉन और प्रोटॉन से बना है। इलेक्ट्रॉन कण होते हैं जो सूर्य के चारों ओर ग्रहों की तरह एक परमाणु के बाहरी आवरण के चारों ओर घूमते हैं।
- परमाणु बहुत छोटा है। सबसे बड़े स्टेडियम की कल्पना करें जिसे आप जानते हैं। यदि स्टेडियम एक परमाणु है, तो इस परमाणु का केंद्रक एक मटर के आकार का होता है।
 3 पता करें कि किसी तत्व की परमाणु संरचना क्या है। एक तत्व प्रकृति में एक पदार्थ है जिसे छोटे पदार्थों में नहीं तोड़ा जा सकता है। तत्व परमाणुओं से बने होते हैं।
3 पता करें कि किसी तत्व की परमाणु संरचना क्या है। एक तत्व प्रकृति में एक पदार्थ है जिसे छोटे पदार्थों में नहीं तोड़ा जा सकता है। तत्व परमाणुओं से बने होते हैं। - तत्व में परमाणु नहीं बदलते हैं। इसका मतलब यह है कि प्रत्येक तत्व की परमाणु संरचना में एक निश्चित संख्या में न्यूट्रॉन और प्रोटॉन होते हैं।
 4 पता करें कि कर्नेल कैसे काम करता है। न्यूक्लियस में न्यूट्रॉन पर न्यूट्रल चार्ज होता है। प्रोटॉन का धनात्मक आवेश होता है। किसी तत्व का परमाणु क्रमांक उसके नाभिक में प्रोटॉनों की संख्या के बराबर होता है..
4 पता करें कि कर्नेल कैसे काम करता है। न्यूक्लियस में न्यूट्रॉन पर न्यूट्रल चार्ज होता है। प्रोटॉन का धनात्मक आवेश होता है। किसी तत्व का परमाणु क्रमांक उसके नाभिक में प्रोटॉनों की संख्या के बराबर होता है.. - नाभिक में प्रोटॉन की संख्या गिनने की कोई आवश्यकता नहीं है। यह संख्या प्रत्येक तत्व के लिए रासायनिक तत्वों की आवर्त सारणी में इंगित की गई है।
 5 नाभिक में न्यूट्रॉन की संख्या की गणना करें। आप आवर्त सारणी से किसी संख्या का उपयोग कर सकते हैं। किसी तत्व का परमाणु क्रमांक नाभिक में प्रोटॉनों की संख्या के बराबर होता है।
5 नाभिक में न्यूट्रॉन की संख्या की गणना करें। आप आवर्त सारणी से किसी संख्या का उपयोग कर सकते हैं। किसी तत्व का परमाणु क्रमांक नाभिक में प्रोटॉनों की संख्या के बराबर होता है। - प्रत्येक तत्व के वर्ग के नीचे उसके नाम के तहत परमाणु द्रव्यमान का संकेत दिया जाता है।
- याद रखें कि परमाणु के नाभिक में केवल प्रोटॉन और न्यूट्रॉन होते हैं। आवर्त सारणी में प्रोटॉनों की संख्या तथा परमाणु भार का मान दर्शाया गया है।
- अब सब कुछ कैलकुलेट करना आसान हो जाएगा। परमाणु द्रव्यमान से प्रोटॉन की संख्या घटाएं और आप तत्व के प्रत्येक परमाणु के नाभिक में न्यूट्रॉन की संख्या प्राप्त करें।
 6 इलेक्ट्रॉनों की संख्या गिनें। याद रखें कि विपरीत आवेश वाले कण आकर्षित करते हैं। इलेक्ट्रॉन धनावेशित होते हैं और परमाणु के चारों ओर चक्कर लगाते हैं। नाभिक की ओर आकर्षित होने वाले ऋणावेशित इलेक्ट्रॉनों की संख्या नाभिक में धनावेशित प्रोटॉनों की संख्या पर निर्भर करती है।
6 इलेक्ट्रॉनों की संख्या गिनें। याद रखें कि विपरीत आवेश वाले कण आकर्षित करते हैं। इलेक्ट्रॉन धनावेशित होते हैं और परमाणु के चारों ओर चक्कर लगाते हैं। नाभिक की ओर आकर्षित होने वाले ऋणावेशित इलेक्ट्रॉनों की संख्या नाभिक में धनावेशित प्रोटॉनों की संख्या पर निर्भर करती है। - चूँकि परमाणु में स्वयं एक तटस्थ आवेश होता है, ऋणात्मक आवेश वाले कणों की संख्या धनात्मक आवेश वाले कणों की संख्या के बराबर होनी चाहिए। इस कारण से, इलेक्ट्रॉनों की संख्या प्रोटॉन की संख्या के बराबर होती है।
 7 तत्वों की आवर्त सारणी देखें। यदि आपके लिए तत्वों के गुण कठिन हैं, तो आवर्त सारणी के बारे में सभी उपलब्ध जानकारी का अध्ययन करें।
7 तत्वों की आवर्त सारणी देखें। यदि आपके लिए तत्वों के गुण कठिन हैं, तो आवर्त सारणी के बारे में सभी उपलब्ध जानकारी का अध्ययन करें। - परीक्षा को सफलतापूर्वक पास करने के लिए आवर्त सारणी को समझना आवश्यक है।
- आवर्त सारणी में केवल तत्व होते हैं। प्रत्येक तत्व का एक वर्णात्मक चिन्ह होता है, यह चिन्ह हमेशा उस तत्व को दर्शाता है। उदाहरण के लिए, Na हमेशा सोडियम होता है। तत्व का पूरा नाम अक्षर चिह्न के नीचे रखा गया है।
- अक्षर चिन्ह के ऊपर की संख्या एक परमाणु संख्या है। यह नाभिक में प्रोटॉनों की संख्या के बराबर होता है।
- अक्षर चिन्ह के नीचे की संख्या परमाणु द्रव्यमान है। याद रखें कि परमाणु द्रव्यमान नाभिक में प्रोटॉन और न्यूट्रॉन का योग है।
 8 स्प्रेडशीट पढ़ना सीखें। तालिका में स्तंभों के रंगों से लेकर बाएं से दाएं और ऊपर से नीचे तक तत्वों की व्यवस्था के बारे में बहुत सारी जानकारी है।
8 स्प्रेडशीट पढ़ना सीखें। तालिका में स्तंभों के रंगों से लेकर बाएं से दाएं और ऊपर से नीचे तक तत्वों की व्यवस्था के बारे में बहुत सारी जानकारी है।
विधि 3 की 5: रासायनिक प्रतिक्रियाओं की गणना
 1 एक समीकरण लिखिए। रसायन विज्ञान की कक्षा में, आपको यह निर्धारित करना सिखाया जाएगा कि तत्वों के संयुक्त होने पर उनका क्या होगा। कागज पर इसे समीकरण हल करना कहते हैं।
1 एक समीकरण लिखिए। रसायन विज्ञान की कक्षा में, आपको यह निर्धारित करना सिखाया जाएगा कि तत्वों के संयुक्त होने पर उनका क्या होगा। कागज पर इसे समीकरण हल करना कहते हैं। - रासायनिक समीकरण में बाईं ओर के पदार्थ, एक तीर और एक प्रतिक्रिया उत्पाद होते हैं। समीकरण के एक तरफ के पदार्थों को दूसरी तरफ के पदार्थों को संतुलित करना चाहिए।
- उदाहरण के लिए, पदार्थ 1 + पदार्थ 2 → उत्पाद 1 + उत्पाद 2।
- टिन (Sn) को ऑक्सीकृत रूप (SnO2) में लें और हाइड्रोजन के साथ गैस (H2) के रूप में मिलाएं। SnO2 + H2 → Sn + H2O।
- यह समीकरण संतुलित होना चाहिए, क्योंकि अभिकर्मक पदार्थों की मात्रा प्राप्त उत्पादों की मात्रा के बराबर होनी चाहिए। दाईं ओर की तुलना में बाईं ओर अधिक ऑक्सीजन परमाणु हैं।
- दो हाइड्रोजन इकाइयों को बाईं ओर और दो पानी के अणुओं को दाईं ओर रखें। अंतिम संस्करण में, संतुलित समीकरण इस तरह दिखता है: SnO2 + 2 H2 → Sn + 2 H2O।
 2 समीकरणों के बारे में नए तरीके से सोचें। यदि आपको समीकरणों को संतुलित करना मुश्किल लगता है, तो कल्पना करें कि यह एक नुस्खा है, लेकिन इसे दोनों तरफ समायोजित करने की आवश्यकता है।
2 समीकरणों के बारे में नए तरीके से सोचें। यदि आपको समीकरणों को संतुलित करना मुश्किल लगता है, तो कल्पना करें कि यह एक नुस्खा है, लेकिन इसे दोनों तरफ समायोजित करने की आवश्यकता है। - टास्क में आपको बाईं ओर सामग्री दी जाती है, लेकिन यह नहीं बताता कि आपको कितनी मात्रा में लेने की जरूरत है। समीकरण यह भी कहता है कि क्या होगा, लेकिन यह नहीं बताता कि कितना होगा। आपको पता लगाने की जरूरत है।
- एक उदाहरण के रूप में पिछले समीकरण का उपयोग करते हुए, SnO2 + H2 → Sn + H2O, आइए सोचें कि यह सूत्र काम क्यों नहीं करेगा। Sn की मात्रा दोनों तरफ समान है, जैसे H2 की मात्रा है, लेकिन बाईं ओर ऑक्सीजन के दो भाग हैं, और दाईं ओर केवल एक है।
- समीकरण के दाहिने पक्ष को बदलना आवश्यक है ताकि परिणामी उत्पाद में H2O के दो भाग हों। H2O के सामने एक दो का मतलब है कि सभी मात्राएँ दोगुनी हो जाएँगी। ऑक्सीजन अब संतुलित है, लेकिन 2 का मतलब है कि अब बाईं ओर की तुलना में दाईं ओर अधिक हाइड्रोजन है। बाईं ओर वापस जाएं और इसके सामने दो रखकर हाइड्रोजन को दोगुना करें।
- अब सब कुछ संतुलन में है। इनपुट मात्रा आउटपुट मात्रा के बराबर है।
 3 समीकरण में और विवरण जोड़ें। रसायन विज्ञान कक्षाओं में, आप उन प्रतीकों से परिचित होंगे जो तत्वों की भौतिक स्थिति को इंगित करते हैं: टी - ठोस, जी - गैस, डब्ल्यू - तरल।
3 समीकरण में और विवरण जोड़ें। रसायन विज्ञान कक्षाओं में, आप उन प्रतीकों से परिचित होंगे जो तत्वों की भौतिक स्थिति को इंगित करते हैं: टी - ठोस, जी - गैस, डब्ल्यू - तरल।  4 रासायनिक प्रतिक्रिया के दौरान होने वाले परिवर्तनों की पहचान करना सीखें। रासायनिक प्रतिक्रियाएं मूल तत्वों या यौगिकों से शुरू होती हैं जो प्रतिक्रिया करते हैं। कनेक्शन के परिणामस्वरूप, एक प्रतिक्रिया उत्पाद या कई उत्पाद प्राप्त होते हैं।
4 रासायनिक प्रतिक्रिया के दौरान होने वाले परिवर्तनों की पहचान करना सीखें। रासायनिक प्रतिक्रियाएं मूल तत्वों या यौगिकों से शुरू होती हैं जो प्रतिक्रिया करते हैं। कनेक्शन के परिणामस्वरूप, एक प्रतिक्रिया उत्पाद या कई उत्पाद प्राप्त होते हैं। - परीक्षा पास करने के लिए, आपको यह जानना होगा कि उन समीकरणों को कैसे हल किया जाए जिनमें अभिकारक या यौगिक उत्पाद, या दोनों हों।
 5 विभिन्न प्रकार की प्रतिक्रियाओं को जानें। रासायनिक प्रतिक्रियाएं विभिन्न कारकों के प्रभाव में हो सकती हैं, और न केवल जब तत्व संयुक्त होते हैं।
5 विभिन्न प्रकार की प्रतिक्रियाओं को जानें। रासायनिक प्रतिक्रियाएं विभिन्न कारकों के प्रभाव में हो सकती हैं, और न केवल जब तत्व संयुक्त होते हैं। - सबसे आम प्रकार की प्रतिक्रियाएं संश्लेषण, विश्लेषण, प्रतिस्थापन, दोहरा अपघटन, एसिड और बेस के बीच प्रतिक्रिया, ऑक्सीकरण-कमी, दहन, आइसोमेराइजेशन, हाइड्रोलिसिस हैं।
- कक्षा में विभिन्न प्रतिक्रियाओं का अध्ययन किया जा सकता है - यह सब पाठ्यक्रम के उद्देश्यों पर निर्भर करता है।विश्वविद्यालय में, सामग्री में गहराई की डिग्री स्कूल के पाठ्यक्रम से भिन्न होगी।
 6 सभी उपलब्ध संसाधनों का उपयोग करें। आपको बुनियादी प्रतिक्रियाओं के बीच के अंतर को समझने की आवश्यकता होगी। इस अंतर को समझने के लिए हर संभव सामग्री का प्रयोग करें। सवाल पूछने से न डरें।
6 सभी उपलब्ध संसाधनों का उपयोग करें। आपको बुनियादी प्रतिक्रियाओं के बीच के अंतर को समझने की आवश्यकता होगी। इस अंतर को समझने के लिए हर संभव सामग्री का प्रयोग करें। सवाल पूछने से न डरें। - रासायनिक अभिक्रियाओं के दौरान क्या परिवर्तन होते हैं, यह समझना इतना आसान नहीं है। यह आपके रसायन शास्त्र वर्ग में सबसे चुनौतीपूर्ण कार्यों में से एक होगा।
 7 प्रतिक्रियाओं के बारे में तर्क के संदर्भ में सोचें। शब्दावली से भ्रमित न होने का प्रयास करें और चीजों को और भी जटिल बनाएं। सभी प्रतिक्रियाओं का उद्देश्य किसी चीज़ को किसी और चीज़ में बदलना है।
7 प्रतिक्रियाओं के बारे में तर्क के संदर्भ में सोचें। शब्दावली से भ्रमित न होने का प्रयास करें और चीजों को और भी जटिल बनाएं। सभी प्रतिक्रियाओं का उद्देश्य किसी चीज़ को किसी और चीज़ में बदलना है। - उदाहरण के लिए, आप पहले से ही जानते हैं कि यदि आप दो हाइड्रोजन परमाणुओं और एक ऑक्सीजन परमाणु - पानी को मिलाते हैं तो क्या होता है। इसलिए, यदि आप सॉस पैन में पानी डालते हैं और आग लगाते हैं, तो कुछ बदल जाएगा। आपने एक रासायनिक प्रतिक्रिया की है। यदि आप फ्रिज में पानी डालते हैं, तो प्रतिक्रिया होगी। आपने कुछ ऐसा बदल दिया जिसमें एक अभिकारक शामिल था, जो कि पानी है।
- प्रत्येक प्रकार की प्रतिक्रिया से तब तक गुजरें जब तक कि आप सब कुछ समझ न लें। ऊर्जा के स्रोत पर ध्यान केंद्रित करें जो प्रतिक्रिया को ट्रिगर करता है और प्रतिक्रिया से होने वाले प्रमुख परिवर्तनों पर ध्यान केंद्रित करता है।
- यदि आपको इसे समझना मुश्किल लगता है, तो समझ से बाहर होने वाली बारीकियों की एक सूची बनाएं और इसे अपने शिक्षक, साथी छात्रों या रसायन विज्ञान में पारंगत किसी भी व्यक्ति को दिखाएं।
5 की विधि 4 : कैलकुलेशन
 1 बुनियादी गणनाओं के क्रम को जानें। रसायन विज्ञान में, कभी-कभी बहुत सटीक गणना की आवश्यकता होती है, लेकिन अक्सर गणित का एक बुनियादी ज्ञान पर्याप्त होता है। यह समझना महत्वपूर्ण है कि गणना किस क्रम में की जाती है।
1 बुनियादी गणनाओं के क्रम को जानें। रसायन विज्ञान में, कभी-कभी बहुत सटीक गणना की आवश्यकता होती है, लेकिन अक्सर गणित का एक बुनियादी ज्ञान पर्याप्त होता है। यह समझना महत्वपूर्ण है कि गणना किस क्रम में की जाती है। - सबसे पहले, गणना कोष्ठक में की जाती है, फिर घातों में गणना, फिर गुणा या भाग, और अंत में - जोड़ या घटाव।
- उदाहरण में 3 + 2 x 6 = ___, सही उत्तर 15 है।
 2 बहुत लंबी संख्याओं को गोल करने से न डरें। रसायन विज्ञान में, वे अक्सर गोल हो जाते हैं, क्योंकि अक्सर एक समीकरण का उत्तर बड़ी संख्या में अंकों के साथ होता है। यदि समस्या विवरण में गोल करने के निर्देश हैं, तो उन्हें ध्यान में रखें।
2 बहुत लंबी संख्याओं को गोल करने से न डरें। रसायन विज्ञान में, वे अक्सर गोल हो जाते हैं, क्योंकि अक्सर एक समीकरण का उत्तर बड़ी संख्या में अंकों के साथ होता है। यदि समस्या विवरण में गोल करने के निर्देश हैं, तो उन्हें ध्यान में रखें। - गोल करना जानते हैं। यदि अगला अंक 4 या उससे कम है, तो इसे नीचे किया जाना चाहिए, यदि 5 या 5 से अधिक है, तो इसे गोल किया जाना चाहिए। उदाहरण के लिए, यहाँ संख्या ६.६६६६६६६६६६६६६६६६ है। टास्क कहता है कि उत्तर को डॉट के बाद दूसरे अंक में गोल करना है। उत्तर 6.67 है।
 3 समझें कि निरपेक्ष मूल्य क्या है। रसायन विज्ञान में, कुछ संख्याओं का एक निरपेक्ष होता है, गणितीय नहीं, अर्थ। एक निरपेक्ष मान शून्य से किसी संख्या तक के सभी मान हैं।
3 समझें कि निरपेक्ष मूल्य क्या है। रसायन विज्ञान में, कुछ संख्याओं का एक निरपेक्ष होता है, गणितीय नहीं, अर्थ। एक निरपेक्ष मान शून्य से किसी संख्या तक के सभी मान हैं। - दूसरे शब्दों में, अब आपके पास नकारात्मक और सकारात्मक मान नहीं हैं, केवल शून्य की दूरी है। उदाहरण के लिए, -20 का निरपेक्ष मान 20 है।
 4 माप की सभी सामान्य इकाइयों को जानें। यहाँ कुछ उदाहरण हैं।
4 माप की सभी सामान्य इकाइयों को जानें। यहाँ कुछ उदाहरण हैं। - किसी पदार्थ की मात्रा को मोल (mol) में मापा जाता है।
- तापमान फ़ारेनहाइट (° F), केल्विन (° K), या सेल्सियस (° C) डिग्री में मापा जाता है।
- द्रव्यमान को ग्राम (जी), किलोग्राम (किलो) या मिलीग्राम (मिलीग्राम) में मापा जाता है।
- तरल की मात्रा लीटर (एल) या मिलीलीटर (एमएल) में मापा जाता है।
 5 एक माप प्रणाली से दूसरे में मूल्यों का अनुवाद करने का अभ्यास करें। परीक्षा में, आपको ऐसे अनुवादों से निपटना होगा। आपको तापमान को एक प्रणाली से दूसरी प्रणाली, पाउंड से किलोग्राम, औंस से लीटर में बदलने की आवश्यकता हो सकती है।
5 एक माप प्रणाली से दूसरे में मूल्यों का अनुवाद करने का अभ्यास करें। परीक्षा में, आपको ऐसे अनुवादों से निपटना होगा। आपको तापमान को एक प्रणाली से दूसरी प्रणाली, पाउंड से किलोग्राम, औंस से लीटर में बदलने की आवश्यकता हो सकती है। - आपको समस्या कथन की इकाइयों के अलावा अन्य इकाइयों में अपना उत्तर देने के लिए कहा जा सकता है। उदाहरण के लिए, समस्या के पाठ में, तापमान डिग्री सेल्सियस में इंगित किया जाएगा, और उत्तर केल्विन डिग्री में आवश्यक होगा।
- आमतौर पर रासायनिक प्रतिक्रियाओं का तापमान केल्विन डिग्री में मापा जाता है। सेल्सियस को फारेनहाइट या केल्विन में बदलने का अभ्यास करें।
 6 जल्दी ना करें। समस्या के पाठ को सोच-समझकर पढ़ें और माप की इकाइयों को परिवर्तित करना सीखें।
6 जल्दी ना करें। समस्या के पाठ को सोच-समझकर पढ़ें और माप की इकाइयों को परिवर्तित करना सीखें।  7 जानिए एकाग्रता की गणना कैसे करें। प्रतिशत, अनुपात और अनुपात की गणना करके बुनियादी गणित के अपने ज्ञान को बेहतर बनाएं।
7 जानिए एकाग्रता की गणना कैसे करें। प्रतिशत, अनुपात और अनुपात की गणना करके बुनियादी गणित के अपने ज्ञान को बेहतर बनाएं।  8 पैकेजिंग पर पोषण संबंधी डेटा के साथ अभ्यास करें। रसायन शास्त्र पास करने के लिए, आपको विभिन्न अनुक्रमों में अनुपात, अनुपात और प्रतिशत की गणना करने में सक्षम होना चाहिए।यदि यह आपके लिए मुश्किल है, तो माप की परिचित इकाइयों में प्रशिक्षण शुरू करें (उदाहरण के लिए, खाद्य पैकेजिंग पर)।
8 पैकेजिंग पर पोषण संबंधी डेटा के साथ अभ्यास करें। रसायन शास्त्र पास करने के लिए, आपको विभिन्न अनुक्रमों में अनुपात, अनुपात और प्रतिशत की गणना करने में सक्षम होना चाहिए।यदि यह आपके लिए मुश्किल है, तो माप की परिचित इकाइयों में प्रशिक्षण शुरू करें (उदाहरण के लिए, खाद्य पैकेजिंग पर)। - पोषण संबंधी डेटा पैक लें। आप प्रति सेवारत कैलोरी की गणना, प्रतिशत के रूप में प्रति दिन अनुशंसित सेवारत, कुल वसा, वसा से कैलोरी का प्रतिशत, कुल कार्ब्स और कार्बोहाइड्रेट प्रकार के अनुसार एक ब्रेकडाउन देखेंगे। इन मानों के आधार पर विभिन्न अनुपातों की गणना करना सीखें।
- उदाहरण के लिए, कुल वसा में मोनोअनसैचुरेटेड वसा की मात्रा की गणना करें। प्रतिशत में बदलें। सर्विंग्स की संख्या और प्रत्येक सर्विंग की कैलोरी सामग्री को जानकर एक पैक में कैलोरी की संख्या की गणना करें। गणना करें कि पैकेज के आधे हिस्से में कितना सोडियम है।
- यह आपको रासायनिक मूल्यों को एक प्रणाली से दूसरी प्रणाली में आसानी से अनुवाद करने में मदद करेगा, उदाहरण के लिए, मोल प्रति लीटर, ग्राम प्रति मोल, और इसी तरह।
 9 अवोगाद्रो की संख्या का उपयोग करना सीखें। यह संख्या एक मोल में अणुओं, परमाणुओं या कणों की संख्या को दर्शाती है। अवोगाद्रो स्थिरांक 6.022x1023 है।
9 अवोगाद्रो की संख्या का उपयोग करना सीखें। यह संख्या एक मोल में अणुओं, परमाणुओं या कणों की संख्या को दर्शाती है। अवोगाद्रो स्थिरांक 6.022x1023 है। - उदाहरण के लिए, Fe के 0.450 मोल में कितने परमाणु होते हैं? उत्तर: 0.450 x 6.022x1023।
 10 गाजर के बारे में सोचो। यदि आपको यह पता लगाना मुश्किल है कि एवोगैड्रो की संख्या का उपयोग कैसे किया जाए, तो परमाणुओं, अणुओं या कणों के बजाय गाजर को गिनने का प्रयास करें। एक दर्जन में कितने गाजर होते हैं? हम जानते हैं कि एक दर्जन 12 होता है, यानी एक दर्जन में 12 गाजर होते हैं।
10 गाजर के बारे में सोचो। यदि आपको यह पता लगाना मुश्किल है कि एवोगैड्रो की संख्या का उपयोग कैसे किया जाए, तो परमाणुओं, अणुओं या कणों के बजाय गाजर को गिनने का प्रयास करें। एक दर्जन में कितने गाजर होते हैं? हम जानते हैं कि एक दर्जन 12 होता है, यानी एक दर्जन में 12 गाजर होते हैं। - अब इस सवाल का जवाब देते हैं कि एक तिल में कितनी गाजर होती है। 12 से गुणा करने के बजाय, हम अवोगाद्रो की संख्या से गुणा करते हैं। एक मोल में 6.022 x 1023 गाजर होती है।
- Avogadro की संख्या का उपयोग परमाणुओं, अणुओं, कणों या गाजर के किसी भी मूल्य को मोल में बदलने के लिए किया जाता है।
- यदि आप किसी पदार्थ के मोलों की संख्या जानते हैं, तो अणुओं, परमाणुओं या कणों की संख्या का मान इस संख्या को अवोगाद्रो की संख्या से गुणा करने के बराबर होगा।
- यह समझना कि कण कैसे मोल्स में परिवर्तित होते हैं, परीक्षा में एक महत्वपूर्ण कारक है। तिल रूपांतरण अनुपात और अनुपात गणना का हिस्सा हैं। इसका मतलब है कि तिल में किसी और चीज के हिस्से के रूप में किसी चीज की मात्रा।
 11 मोलरिटी को समझें। किसी द्रव में किसी पदार्थ के मोलों की संख्या पर विचार करें। इस उदाहरण को समझना बहुत जरूरी है क्योंकि हम मोलरिटी की बात कर रहे हैं, यानी किसी पदार्थ का अनुपात मोल प्रति लीटर में व्यक्त किया जाता है।
11 मोलरिटी को समझें। किसी द्रव में किसी पदार्थ के मोलों की संख्या पर विचार करें। इस उदाहरण को समझना बहुत जरूरी है क्योंकि हम मोलरिटी की बात कर रहे हैं, यानी किसी पदार्थ का अनुपात मोल प्रति लीटर में व्यक्त किया जाता है। - मोलरिटी, या मोलर सांद्रण, एक ऐसा शब्द है जो किसी तरल पदार्थ में किसी पदार्थ की मात्रा को व्यक्त करता है, अर्थात किसी घोल में विलेय की मात्रा। मोलरिटी प्राप्त करने के लिए, आपको विलेय के मोल को लीटर घोल से विभाजित करना होगा। मोलरता मोल प्रति लीटर में व्यक्त की जाती है।
- घनत्व की गणना करें। घनत्व अक्सर रसायन शास्त्र में प्रयोग किया जाता है। घनत्व प्रति इकाई आयतन एक रसायन का द्रव्यमान है। आमतौर पर, घनत्व ग्राम प्रति मिलीलीटर या ग्राम प्रति घन सेंटीमीटर में व्यक्त किया जाता है - यह वही बात है।
 12 समीकरणों को एक अनुभवजन्य सूत्र में कम करें। इसका मतलब है कि उत्तर तभी सही होगा जब आप सभी मूल्यों को उनके सरलतम रूप में लाएंगे।
12 समीकरणों को एक अनुभवजन्य सूत्र में कम करें। इसका मतलब है कि उत्तर तभी सही होगा जब आप सभी मूल्यों को उनके सरलतम रूप में लाएंगे। - यह आणविक सूत्रों पर लागू नहीं होता है, क्योंकि वे अणु बनाने वाले रासायनिक तत्वों के सटीक अनुपात को इंगित करते हैं।
 13 जानिए आणविक सूत्र में क्या शामिल है। आणविक सूत्र को सबसे सरल, या अनुभवजन्य रूप में लाने की आवश्यकता नहीं है, क्योंकि यह कहता है कि अणु वास्तव में किससे बना है।
13 जानिए आणविक सूत्र में क्या शामिल है। आणविक सूत्र को सबसे सरल, या अनुभवजन्य रूप में लाने की आवश्यकता नहीं है, क्योंकि यह कहता है कि अणु वास्तव में किससे बना है। - आणविक सूत्र तत्वों के संक्षिप्त रूप और अणु में प्रत्येक तत्व के परमाणुओं की संख्या का उपयोग करके लिखा जाता है।
- उदाहरण के लिए, पानी का आणविक सूत्र H2O है। इसका मतलब है कि पानी के प्रत्येक अणु में दो हाइड्रोजन परमाणु और एक ऑक्सीजन परमाणु होता है। एसिटामिनोफेन का आणविक सूत्र C8H9NO2 है। प्रत्येक रासायनिक यौगिक का एक आणविक सूत्र होता है।
 14 याद रखें कि रसायन विज्ञान में गणित को स्टोइकोमेट्री कहा जाता है। आप इस अवधि के पार आ जाएंगे। यह इस बात का विवरण है कि गणितीय सूत्रों में रसायन विज्ञान को कैसे व्यक्त किया जाता है। रासायनिक गणित, या स्टोइकोमेट्री में, तत्वों और रासायनिक यौगिकों की मात्रा अक्सर मोल्स में, मोल में प्रतिशत, मोल प्रति लीटर या मोल प्रति किलोग्राम में व्यक्त की जाती है।
14 याद रखें कि रसायन विज्ञान में गणित को स्टोइकोमेट्री कहा जाता है। आप इस अवधि के पार आ जाएंगे। यह इस बात का विवरण है कि गणितीय सूत्रों में रसायन विज्ञान को कैसे व्यक्त किया जाता है। रासायनिक गणित, या स्टोइकोमेट्री में, तत्वों और रासायनिक यौगिकों की मात्रा अक्सर मोल्स में, मोल में प्रतिशत, मोल प्रति लीटर या मोल प्रति किलोग्राम में व्यक्त की जाती है। - आपको ग्राम को मोल में बदलना होगा।किसी तत्व की इकाई का ग्राम में परमाणु द्रव्यमान इस पदार्थ के एक मोल के बराबर होता है। उदाहरण के लिए, कैल्शियम का परमाणु द्रव्यमान 40 परमाणु द्रव्यमान इकाई है। इस प्रकार, 40 ग्राम कैल्शियम एक मोल कैल्शियम के बराबर होता है।
 15 अतिरिक्त असाइनमेंट के लिए पूछें। यदि समीकरण और रूपांतरण आपके लिए कठिन हैं, तो अपने शिक्षक से बात करें। अधिक कार्यों के लिए पूछें ताकि आप स्वयं उन पर तब तक काम कर सकें जब तक आप सभी घटनाओं का सार नहीं समझ लेते।
15 अतिरिक्त असाइनमेंट के लिए पूछें। यदि समीकरण और रूपांतरण आपके लिए कठिन हैं, तो अपने शिक्षक से बात करें। अधिक कार्यों के लिए पूछें ताकि आप स्वयं उन पर तब तक काम कर सकें जब तक आप सभी घटनाओं का सार नहीं समझ लेते।
विधि 5 की 5: रसायन विज्ञान की भाषा
 1 लुईस चार्ट को समझना सीखें। लुईस चार्ट को कभी-कभी स्कैटर चार्ट कहा जाता है। ये सरल आरेख हैं, जिनमें बिंदु एक परमाणु के बाहरी कोश में मुक्त और बाध्य इलेक्ट्रॉनों का प्रतिनिधित्व करते हैं।
1 लुईस चार्ट को समझना सीखें। लुईस चार्ट को कभी-कभी स्कैटर चार्ट कहा जाता है। ये सरल आरेख हैं, जिनमें बिंदु एक परमाणु के बाहरी कोश में मुक्त और बाध्य इलेक्ट्रॉनों का प्रतिनिधित्व करते हैं। - ऐसी प्रणाली आपको सरल आरेख बनाने की अनुमति देती है जो एक परमाणु या अणु में तत्वों के बीच के बंधन को दर्शाती है, उदाहरण के लिए, सहसंयोजक।
 2 जानिए क्या है अष्टक नियम। लुईस आरेखों का निर्माण करते समय, ऑक्टेट नियम का उपयोग किया जाता है, जिसमें कहा गया है कि एक परमाणु स्थिर हो जाता है जब उसके बाहरी आवरण में आठ इलेक्ट्रॉनों तक पहुंच होती है। हाइड्रोजन एक अपवाद है - बाहरी कोश में दो इलेक्ट्रॉन होने पर इसे स्थिर माना जाता है।
2 जानिए क्या है अष्टक नियम। लुईस आरेखों का निर्माण करते समय, ऑक्टेट नियम का उपयोग किया जाता है, जिसमें कहा गया है कि एक परमाणु स्थिर हो जाता है जब उसके बाहरी आवरण में आठ इलेक्ट्रॉनों तक पहुंच होती है। हाइड्रोजन एक अपवाद है - बाहरी कोश में दो इलेक्ट्रॉन होने पर इसे स्थिर माना जाता है।  3 लुईस आरेख खींचिए। तत्व का अक्षर चिन्ह डॉट्स से घिरा हुआ है और एक लुईस आरेख है। कल्पना कीजिए कि आरेख एक मूवी फ्रेम है। इलेक्ट्रॉन तत्वों के बाहरी आवरण के चारों ओर चक्कर नहीं लगाते - वे एक निश्चित अवधि में परावर्तित होते हैं।
3 लुईस आरेख खींचिए। तत्व का अक्षर चिन्ह डॉट्स से घिरा हुआ है और एक लुईस आरेख है। कल्पना कीजिए कि आरेख एक मूवी फ्रेम है। इलेक्ट्रॉन तत्वों के बाहरी आवरण के चारों ओर चक्कर नहीं लगाते - वे एक निश्चित अवधि में परावर्तित होते हैं। - आरेख इलेक्ट्रॉनों के स्थिर द्रव्यमान को दर्शाता है, जहां वे किसी अन्य तत्व से जुड़े होते हैं, और बांड के बारे में जानकारी (उदाहरण के लिए, क्या बांड को दोगुना किया जाता है और कई इलेक्ट्रॉनों के बीच साझा किया जाता है)।
- ऑक्टेट नियम के बारे में सोचें और एक तत्व प्रतीक की कल्पना करें - उदाहरण के लिए, सी (कार्बन)। प्रतीक के पूर्व, पश्चिम, उत्तर और दक्षिण में प्रत्येक में दो बिंदु बनाएं। अब प्रत्येक बिंदु के प्रत्येक तरफ एक एच (हाइड्रोजन परमाणु) प्रतीक बनाएं। आरेख से पता चलता है कि प्रत्येक कार्बन परमाणु चार हाइड्रोजन परमाणुओं से घिरा हुआ है। उनके इलेक्ट्रॉन सहसंयोजी रूप से बंधित होते हैं, अर्थात कार्बन और हाइड्रोजन परमाणुओं के लिए, इलेक्ट्रॉनों में से एक दूसरे तत्व के एक इलेक्ट्रॉन से बंधा होता है।
- ऐसे यौगिक का आणविक सूत्र CH4 है। यह मीथेन गैस है।
 4 समझें कि इलेक्ट्रॉन तत्वों को कैसे बांधते हैं। लुईस आरेख एक सरल रूप में रासायनिक बंधों का प्रतिनिधित्व करते हैं।
4 समझें कि इलेक्ट्रॉन तत्वों को कैसे बांधते हैं। लुईस आरेख एक सरल रूप में रासायनिक बंधों का प्रतिनिधित्व करते हैं। - अपने शिक्षक और सहपाठियों के साथ इस विषय पर चर्चा करें यदि आप यह नहीं समझते हैं कि तत्व कैसे जुड़े हुए हैं और लुईस आरेख क्या दर्शाते हैं।
 5 पता करें कि कनेक्शन क्या कहलाते हैं। रसायन विज्ञान की शब्दावली के अपने नियम हैं। प्रतिक्रियाओं के प्रकार, बाहरी शेल में इलेक्ट्रॉनों की हानि या लाभ, और तत्वों की स्थिरता या अस्थिरता रसायन विज्ञान की शब्दावली का हिस्सा हैं।
5 पता करें कि कनेक्शन क्या कहलाते हैं। रसायन विज्ञान की शब्दावली के अपने नियम हैं। प्रतिक्रियाओं के प्रकार, बाहरी शेल में इलेक्ट्रॉनों की हानि या लाभ, और तत्वों की स्थिरता या अस्थिरता रसायन विज्ञान की शब्दावली का हिस्सा हैं।  6 इसे गंभीरता से लें। कई केमिस्ट्री कोर्सेज में इसके लिए अलग-अलग चैप्टर होते हैं। अक्सर, शब्दावली न जानने का अर्थ है परीक्षा में असफल होना।
6 इसे गंभीरता से लें। कई केमिस्ट्री कोर्सेज में इसके लिए अलग-अलग चैप्टर होते हैं। अक्सर, शब्दावली न जानने का अर्थ है परीक्षा में असफल होना। - यदि संभव हो तो कक्षा से पहले शब्दावली का अध्ययन करें। आप एक नियमित किताबों की दुकान या इंटरनेट पर विशेष साहित्य खरीद सकते हैं।
 7 जानिए रेखा के ऊपर और नीचे की संख्याओं का क्या मतलब है। यह रसायन शास्त्र सीखने का एक बहुत ही महत्वपूर्ण हिस्सा है।
7 जानिए रेखा के ऊपर और नीचे की संख्याओं का क्या मतलब है। यह रसायन शास्त्र सीखने का एक बहुत ही महत्वपूर्ण हिस्सा है। - रेखा के ऊपर की संख्याओं को तत्वों की आवर्त सारणी में देखा जा सकता है। वे किसी तत्व या रासायनिक यौगिक के कुल आवेश का प्रतिनिधित्व करते हैं। आवर्त सारणी और ऊर्ध्वाधर पंक्तियों में तत्वों की जांच करें जिनकी सूचकांक संख्या समान है।
- रेखा के नीचे की संख्याओं का उपयोग यौगिक में जाने वाले प्रत्येक तत्व की मात्रा का वर्णन करने के लिए किया जाता है। जैसा कि पहले उल्लेख किया गया है, H2O सूत्र में 2 इंगित करता है कि पानी के अणु में दो हाइड्रोजन परमाणु हैं।
 8 समझें कि परमाणु एक दूसरे के साथ कैसे प्रतिक्रिया करते हैं। शब्दावली में, विशेष नियम हैं जिनका पालन कुछ प्रकार की प्रतिक्रियाओं के उत्पादों का नामकरण करते समय किया जाना चाहिए।
8 समझें कि परमाणु एक दूसरे के साथ कैसे प्रतिक्रिया करते हैं। शब्दावली में, विशेष नियम हैं जिनका पालन कुछ प्रकार की प्रतिक्रियाओं के उत्पादों का नामकरण करते समय किया जाना चाहिए। - प्रतिक्रियाओं में से एक ऑक्सीकरण-कमी है। प्रतिक्रिया के दौरान, या तो इलेक्ट्रॉनों का अधिग्रहण या हानि होती है।
- ऑक्सीकरण के दौरान इलेक्ट्रॉन खो जाते हैं और अपचयन के दौरान अधिग्रहित हो जाते हैं।
 9 याद रखें कि रेखा के नीचे की संख्याएं यौगिक के स्थिर आवेश सूत्र को इंगित कर सकती हैं। एक यौगिक के अंतिम आणविक सूत्र का वर्णन करने के लिए वैज्ञानिक इस तरह की संख्याओं का उपयोग करते हैं, जो एक तटस्थ चार्ज के साथ एक स्थिर यौगिक को भी दर्शाता है।
9 याद रखें कि रेखा के नीचे की संख्याएं यौगिक के स्थिर आवेश सूत्र को इंगित कर सकती हैं। एक यौगिक के अंतिम आणविक सूत्र का वर्णन करने के लिए वैज्ञानिक इस तरह की संख्याओं का उपयोग करते हैं, जो एक तटस्थ चार्ज के साथ एक स्थिर यौगिक को भी दर्शाता है। - एक तटस्थ आवेश प्राप्त करने के लिए, एक धनावेशित आयन, जिसे एक धनायन कहा जाता है, को ऋणात्मक आयन, एक आयन से समान आवेश के साथ संतुलित किया जाना चाहिए। ये शुल्क रेखा के नीचे लिखे गए हैं।
- उदाहरण के लिए, मैग्नीशियम आयन में +2 धनायन का आवेश होता है, और नाइट्रोजन आयन में -3 आयन का आवेश होता है। +2 और -3 को लाइन के नीचे दर्शाया गया है। एक तटस्थ चार्ज प्राप्त करने के लिए, नाइट्रोजन की प्रत्येक 2 इकाइयों के लिए, आपको मैग्नीशियम के 3 परमाणुओं का उपयोग करने की आवश्यकता होती है।
- सूत्र में, यह इस प्रकार लिखा गया है: Mg3N2
 10 तत्वों की आवर्त सारणी में आयनों और धनायनों को उनकी स्थिति से पहचानना सीखें। तालिका के तत्व जो पहले कॉलम में हैं, वे क्षार धातु हैं और उन पर +1 धनायन आवेश है। उदाहरण के लिए, ना + और ली +।
10 तत्वों की आवर्त सारणी में आयनों और धनायनों को उनकी स्थिति से पहचानना सीखें। तालिका के तत्व जो पहले कॉलम में हैं, वे क्षार धातु हैं और उन पर +1 धनायन आवेश है। उदाहरण के लिए, ना + और ली +। - दूसरे स्तंभ में क्षारीय पृथ्वी धातुओं में 2+ धनायन आवेश होता है, जैसे Mg2 + और Ba2 +।
- सातवें स्तंभ के तत्वों को हैलोजन कहा जाता है और इनमें Cl- और I- जैसे आयनों का -1 आवेश होता है।
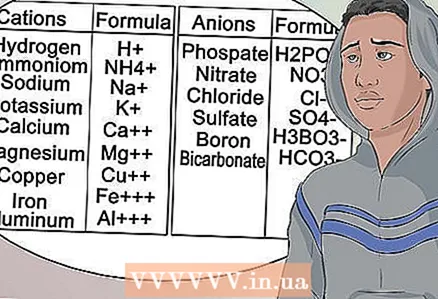 11 आम आयनों और धनायनों को पहचानना सीखें। परीक्षा पास करने के लिए, आइटम समूहों से जुड़ी सभी शब्दावली सीखें। रेखा के निचले भाग में ये संख्याएँ नहीं बदलती हैं।
11 आम आयनों और धनायनों को पहचानना सीखें। परीक्षा पास करने के लिए, आइटम समूहों से जुड़ी सभी शब्दावली सीखें। रेखा के निचले भाग में ये संख्याएँ नहीं बदलती हैं। - दूसरे शब्दों में, मैग्नीशियम हमेशा +2 धनायन आवेश के साथ Mg होता है।
 12 जानकारी से भ्रमित न होने का प्रयास करें। विभिन्न प्रकार की रासायनिक प्रतिक्रियाओं की जानकारी, इलेक्ट्रॉनों के आदान-प्रदान के बारे में, किसी तत्व या उसके घटक के आवेश में परिवर्तन के बारे में जानकारी आपके पास से गुजरेगी, और यह सब आत्मसात करना मुश्किल होगा।
12 जानकारी से भ्रमित न होने का प्रयास करें। विभिन्न प्रकार की रासायनिक प्रतिक्रियाओं की जानकारी, इलेक्ट्रॉनों के आदान-प्रदान के बारे में, किसी तत्व या उसके घटक के आवेश में परिवर्तन के बारे में जानकारी आपके पास से गुजरेगी, और यह सब आत्मसात करना मुश्किल होगा। - कठिन विषयों को टुकड़ों में तोड़ें। उदाहरण के लिए, यदि आप ऑक्सीकरण प्रतिक्रिया या सकारात्मक और नकारात्मक चार्ज वाले तत्वों के संयोजन के सिद्धांत को नहीं समझते हैं, तो आप जो भी जानकारी जानते हैं उसे बोलना शुरू करें, और आप समझ जाएंगे कि आप पहले से ही बहुत कुछ समझने और याद रखने में कामयाब रहे हैं।
 13 अपने शिक्षक के साथ नियमित रूप से चैट करें। कठिन विषयों की एक सूची बनाएं और अपने शिक्षक से आपकी मदद करने के लिए कहें। इससे आपको समूह के अगले विषय पर आगे बढ़ने से पहले सामग्री को आंतरिक करने का मौका मिलेगा, जो आपको और भ्रमित करेगा।
13 अपने शिक्षक के साथ नियमित रूप से चैट करें। कठिन विषयों की एक सूची बनाएं और अपने शिक्षक से आपकी मदद करने के लिए कहें। इससे आपको समूह के अगले विषय पर आगे बढ़ने से पहले सामग्री को आंतरिक करने का मौका मिलेगा, जो आपको और भ्रमित करेगा।  14 कल्पना कीजिए कि रसायन शास्त्र एक नई भाषा सीखने जैसा है। यह समझना महत्वपूर्ण है कि लेखन शुल्क, एक अणु में परमाणुओं की संख्या और अणुओं के बीच का बंधन रसायन विज्ञान की भाषा का हिस्सा है। यह सब दर्शाता है कि कागज पर प्रकृति में क्या होता है।
14 कल्पना कीजिए कि रसायन शास्त्र एक नई भाषा सीखने जैसा है। यह समझना महत्वपूर्ण है कि लेखन शुल्क, एक अणु में परमाणुओं की संख्या और अणुओं के बीच का बंधन रसायन विज्ञान की भाषा का हिस्सा है। यह सब दर्शाता है कि कागज पर प्रकृति में क्या होता है। - यह सब समझना बहुत आसान होगा यदि सभी प्रक्रियाओं को लाइव देखा जा सकता है। आपके लिए न केवल प्रक्रियाओं के सिद्धांतों को समझना महत्वपूर्ण है, बल्कि इस जानकारी को रिकॉर्ड करने के लिए उपयोग की जाने वाली भाषा भी है।
- यदि आपको रसायन शास्त्र का अध्ययन करना कठिन लगता है, तो याद रखें कि आप अकेले हैं और हार न मानें। अपने प्रशिक्षक, समूह या किसी ऐसे व्यक्ति से बात करें जो इस विषय में पारंगत हो। यह सब सीखा जा सकता है, लेकिन यह अधिक सही होगा यदि कोई आपको सामग्री समझा सके ताकि आप सब कुछ समझ सकें।
टिप्स
- आराम करना न भूलें। अपनी पढ़ाई से ब्रेक लेने से आप नए सिरे से स्कूल लौट पाएंगे।
- परीक्षा की पूर्व संध्या पर कुछ नींद लें। एक सोए हुए व्यक्ति की याददाश्त और एकाग्रता बेहतर होती है।
- जो आप पहले से जानते हैं उसे दोबारा पढ़ें। रसायन विज्ञान एक घटना के अध्ययन और ज्ञान के विस्तार पर निर्मित विज्ञान है। आपने जो कुछ भी सीखा है उसे याद रखना महत्वपूर्ण है ताकि परीक्षा के प्रश्न आपको आश्चर्यचकित न करें।
- कक्षा के लिए तैयार हो जाओ। सभी सामग्री पढ़ें और अपना गृहकार्य करें। अगर आप किसी चीज को मिस करते हैं तो आप ज्यादा से ज्यादा पीछे रह जाएंगे।
- समय आवंटित करें। रसायन शास्त्र पर अधिक ध्यान दें यदि यह विषय आपके लिए अच्छा नहीं है, लेकिन अपना सारा समय इसमें न दें, क्योंकि अन्य विषय भी हैं।



